Насыщенные жиры | Насыщенные жирные кислоты
Обратно в Состав продуктовНасыщенные (или предельные жирные кислоты) – это одноосновные жирные кислоты, в структуре которых отсутствуют двойные связи между соседними атомами углерода. Отсутствие двойных, или ненасыщенных, связей заметно снижает реакционную способность насыщенных жирных кислот.
В пищевых продуктах эти вещества встречаются в составе жиров как животного, так и растительного происхождения.
Содержание насыщенных жирных кислот в жирах животного происхождения, как правило, выше, чем в растительных жирах. В этой связи следует отметить четкую закономерность: чем больше жир содержит насыщенных жирных кислот, тем выше у него температура плавления. То есть, если сравнивать подсолнечное и сливочное масло, то сразу становится понятно, что у твердого сливочного содержание насыщенных жирных кислот значительно выше.
Примером насыщенного жира растительного происхождения служит пальмовое масло, польза и вред которого активно обсуждаются в современном обществе.
Примером ненасыщенного животного жира является рыбий. Бывают также искусственные насыщенные жиры, полученные гидрогенизацией ненасыщенных. Гидрогенизированный жир составляет основу маргарина.
Наиболее значительными представителями насыщенных жирных кислот являются стеариновая (например, в бараньем жире ее содержание достигает 30%, а в растительных маслах – до 10%) и пальмитиновая (ее содержание в пальмовом масле составляет 39-47%, в коровьем – около 25%, соевом – 6,5%, а в свином сале – 30%) кислоты. Другими представителями насыщенных жирных кислот являются лауриновая, миристиновая, маргариновая, каприновая и др. кислоты.
Биологическая роль насыщенных жирных кислот заключается том, что они для организма человека являются, прежде всего, источником энергии. Также они принимают участие в построении клеточных мембран, синтезе гормонов, переносе и усвоении витаминов и микроэлементов. Имеющие мало жировой ткани женщины не только намного чаще страдают бесплодием в репродуктивном возрасте, но и сложнее переносят климакс, страдая болезнями и стрессами из-за гормонального дисбаланса.
С другой стороны, вред избытка жировой ткани, т.е. ожирения, также не вызывает сомнений. В современных условиях гиподинамии и переедания человек должен стремиться к снижению насыщенных жирных кислот в своем рационе – энергетическая ценность рациона и так, как правило, находится выше нормы, а необходимые для построения клеточных мембран жирные кислоты могут быть синтезированы организмом (при условии соблюдения достаточной энергетической ценности рациона). Чрезмерное потребление насыщенных жиров является одним из важнейших факторов риска развития ожирения, диабета, сердечно-сосудистых и др. заболеваний. Нормы потребления для насыщенных жиров не установлены, однако считается, что их энергетическая ценность в рационе в норме не должна составлять более 10%.
Однако в суровых климатических условиях, например, на Крайнем Севере, необходимость в энергии резко возрастает, поэтому требуется введение в рацион большего количества жиров, содержащих в т. ч. насыщенные жирные кислоты – наиболее энергетически ценный компонент.
Если ненасыщенные жиры полезнее насыщенных с точки зрения питания, то в области кулинарии всё наоборот: готовить еду лучше на животных жирах или маргарине. При жарке пищи на растительном масле двойные связи ненасыщенных жирных кислот будут подвергаться интенсивному окислению с образованием канцерогенных веществ, вызывающих рак.
Важнейшая непищевая область применения насыщенных жирных кислот – мыловарение. Натриевые и калиевые соли этих соединений составляют основу всех видов мыла. Собственно, мыло и получают путем омыления соответствующих насыщенных жиров.
Обратно в Состав продуктов
Состав жиров и жирные кислоты
Жиры представляют собой сложный комплекс органических соединений, основными структурными элементами которых являются глицерин и жирные кислоты.
Удельный вес глицерина в составе жиров незначительный.
Количество его не превышает 10 %.
Основное значение, определяющее свойства жиров, имеют жирные кислоты.
В составе жиров находится ряд веществ, из которых наибольшее физиологическое значение имеют фосфатиды, стерины и жирорастворимые витамины.
Жирные кислоты
В природных жирах жирные кислоты встречаются в большом разнообразии, их около 60 наименований.
Все жирные кислоты, входящие в состав пищевых жиров, содержат четное число углеродных атомов.
Жирные кислоты подразделяются на предельные (насыщенные) и непредельные (ненасыщенные).
Предельные (насыщенные) жирные кислоты
Предельные жирные кислоты в большом количестве встречаются в составе животных жиров.
Предельные жирные кислоты, входящие в состав животных жиров
| Жирная кислота | Молекулярный вес | Температура плавления в °C |
|---|---|---|
| Масляная | 88 | -7,9 |
| Капроновая | 116 | -1,5 |
| Каприловая | 144 | +16,7 |
| Каприновая | 172 | +31,6 |
| Миристиновая | 228 | +53,9 |
| Лауриновая | 200 | +44,2 |
| Пальмитиновая | 256 | +62,6 |
| Стеариновая | 284 | +69,3 |
| Арахиновая | 312 | +74,9 |
| Бегеновая | 340 | +79,7 |
| Лигноцериновая | 368 | +83,9 |
| Церотиновая | 396 | +87,7 |
| Монтановая | 424 | +90,4 |
| Мелиссиновая | 452 | +93,6 |
Из предельных жирных кислот наиболее распространены
- пальмитиновая [CH3(CH2)14COOH]
- стеариновая [CH3(CH2)16COOH]
- миристиновая [CH3(CH2)12COOH]
- масляная [CH3(CH2)2COOH]
- капроновая [CH3(CH2)4COOH]
- каприловая [CH3(CH2)6COOH]
- каприновая [CH3(CH2)8COOH]
- арахиновая [Ch4(CH2)18COOH]
Высокомолекулярные насыщенные кислоты (стеариновая, арахиновая, пальмитиновая) обладают твердой консистенцией, низкомолекулярные (масляная, капроновая и др.) — жидкой. От молекулярного веса зависит и температура плавления. Чем выше молекулярный вес насыщенных жирных кислот, тем выше их температура плавления.
Разные жиры содержат различные количества жирных кислот. Так, в кокосовом масле 9 жирных кислот, в льняном — 6. Это обусловливает образование эвтектических смесей, т. е. сплавов, обладающих температурой плавления, как правило, более низкой, чем температура плавления составляющих компонентов. Наличие в пищевых жирах смесей триглицеридов имеет важное физиологическое значение: они снижают температуру плавления жира и тем самым способствуют его эмульгированию в двенадцатиперстной кишке и лучшему усвоению.
Насыщенные (предельные) жирные кислоты в большом количестве (более 50 %) содержатся в животных жирах (бараньем, говяжьем и др.) и в некоторых растительных маслах (кокосовом, пальмоядровом).
По биологическим свойствам предельные жирные кислоты уступают непредельным. С предельными (насыщенными) жирными кислотами скорее связываются представления об отрицательном их влиянии на жировой обмен, на функцию и состояние печени, а также со способствующей их ролью в развитии атеросклероза.
Имеются данные о том, что повышение содержания холестерина в крови в большей степени связано с высококалорийным питанием и одновременным поступлением животных жиров, богатых предельными жирными кислотами.
Жирные кислоты предельные — Справочник химика 21
Карбоновые кислоты. Строение карбоксильной группы. Одноосновные предельные кислоты. Изомерия и номенклатура. Физические и химические свойства. Индуктивный эффект. Функциональные пройзводные карбоновых кислот галогенангидриды, ангидриды, эфиры, амиды, гидропероксиды и пероксиды. Высшие жирные кислоты (ВЖК). Мыла. Одноосновные непредельные кислоты и их свойства. Двухосновные предельные и непредельные кислоты. Отдельные представители карбоновых кислот. УФ и ИК спектры карбоновых кислот. [c.170]Из природных жиров для приготовления пищи чаще всего используют сливочное масло (жир, содержащийся в молоке) и животный жир — сало, а из растительных масел — оливковое и арахисовое. Такие жиры и масла обычно гораздо дороже, чем Некоторые растительные масла, которые не годятся в пищу. Например, семена хлопчатника примерно на 25% состоят из масла. Если учесть, сколько хлопка выращивается в нашей стране, можно представить себе, сколько можно было бы добыть из его семян хлопкового масла. Но его нельзя употреблять в пищу из-за неприятного привкуса. Причина этого привкуса — непредельные жирные кислоты, которые входят в состав его молекул. Если же хлопковое мае ло при определенных условиях обработать водородом, его атомы присоединяются к двойным связям непредельных кислот, и они превратятся в предельные. В результате получается твердый жир, вполне пригодный для при— готовления пищи. Подобные кулинарные жиры, полученные из растительных масел, в наше время нашли довольно широкое применение.
Температура плавления жирных кислот зависит, однако, не только от длины углеродной цепи. В молекуле стеариновой кислоты, как я уже говорил, 18 атомов углерода. При этом все они соединены между собой одинарными связями, стеариновая кислота является предельной. [c.159]
Предельные жирные кислоты человеческий организм может без особого труда вырабатывать самостоятельно. (Именно поэтому люди так толстеют от пищи, содержащей много крахмала. Организм расщепляет крахмал до уксусной кислоты, а потом синтезирует из нее жирные кислоты, которые включаются в молекулы жира.) Организм может также удваивать одну из связей в молекуле- жирной кислоты и получать собственную олеиновую кислоту. Но вот несколько двойных связей организм ввести в молекулу не может. [c.160]
Гидрирование жиров. Жиры животного и растительного происхождения состоят в основном из триглицеридов предельных и непредельных карбоновых кислот. В некоторых жирах встречаются эфиры высокомолекулярных жирных кислот и высокомолекулярных спиртов алифатического ряда. В качестве примесей могут быть соединения фосфора, азота и серы.
Молекулы жиров и масел представляют собой сложные эфиры глицерина, и называются они глицеридами. Образуя их, каждая из трех гидроксильных групп глицерина конденсируется с карбоксильной группой жирной кислоты. Эти жирные кислоты могут иметь цепь длиной от 4 до 24 атомов углерода. Они могут быть предельными или иметь от одной до пяти двойных связей. Естественно, каждая молекула жира с определенным набором жирных кислот отличается от молекул с немного другим набором. А природные жиры и масла — это не что иное, как сложные смеси различных глицеридов. [c.197]
В присутствии сероводорода превращение отмерших водорослей происходит при бактериальном воздействии только в анаэробных условиях на дне водоема. При этом жирные кислоты, предельные и непредельные, отщепляют углекислоту и превращаются в углеводороды. Если такой декарбоксилированный материал по каким-либо причинам выносится на поверхность воды, то непредельные соединения полимеризуются, в результате чего образуется твердая упругая масса, в которой неравномерно распределены скопления жидких углеводородов, отделившиеся от всей массы путем синерезиса. Так образуется куронгит в лагунах и солоноводных озерах Австралии. [c.104]
Описанным методом от жидких жирных кислот отделяют все твердые высокомолекулярные предельные жирные кислоты, предельные оксикислоты и двухосновные кислоты. Некоторое количество свинцовых солей твердых непредельных кислот и пальмитиновой кислоты переходит вместе с солями жидких кислот в спиртовой раствор вследствие частичной растворимости их свинцовых солей в спирте. [c.155]
В состав растительных и животных жиров входят различные насыщенные и ненасыщенные жирные кислоты и их глицериды, причем предельные кислоты и их глицериды преобладают в твердых (в частности, в животных) жирах, а непредельные — в жидких — (растительных). Наличие в жирах непредельных соединений приводит к получению менее химически стабильного загустителя, склонного к окислению и разложению. [c.188]
После открытия Марковниковым и Оглоблиным [3] в бакинских нефтях нового обширного класса предельных углеводородов циклопарафинов, который они назвали нафтенами, и выделенные из этих нефтей кислоты состава С Н2п—2О2 или С Н2п—1 СООН получили название нафтеновые кислоты. Это обш ее название нефтяных карбоновых кислот сохранилось до настоящего времени, несмотря на то, что уже в самых ранних работах было показано, что среди нефтяных кислот присутствуют и низшие жирные кислоты. [c.305]
Существенное влияние на срок службы катализатора и состав спиртов, получаемых в процессе прямого гидрирования. СШК, оказывает качество исходных кислот. В составе выпускаемых ныне синтетических жирных кислот содержание углеводородов достигает 2,5—3,5%, т. е. половины того предельного содержания их, которое допустимо временными техническими условиями на спирты. Таким образом, количество углеводородов, образующихся непосредственно в процессе гидрирования, не должно превышать [c.183]
Предельные жирные кислоты, входящие в состав жиров, четные. В небольших количествах встречаются масляная, капроновая и каприловая кислоты. [c.43]
Водород поступает в низ колонны также через распылитель. В колонне бутиловые эфиры жирных кислот в присутствии катализатора вступают Ео взаимодействие с водородом и образуют жирные спирты. Наряду с образованием жирных спиртов происходит насыщение непредельных жирных кислот до предельных и частичное образование углеводородов.
Жирные кислоты — это… Что такое Жирные кислоты?
Жирные кислоты — алифатические одноосновные карбоновые кислоты с открытой цепью, содержащиеся в этерифицированной форме в жирах, маслах и восках растительного и животного происхождения. Жирные кислоты, как правило, содержат неразветвленную цепь из четного числа атомов углерода (С4-24, включая карбоксильный углерод) и могут быть как насыщенными, так и ненасыщенными[1].
Общие сведения
Жирные кислоты могут быть насыщенными (только с одинарными связями между атомами углерода), мононенасыщенными (с одной двойной связью между атомами углерода) и полиненасыщенными (с двумя и более двойными связями, находящимися, как правило, через CH2-группу). Они различаются по количеству углеродных атомов в цепи, а также, в случае ненасыщенных кислот, по положению, конфигурации (как правило цис-) и количеству двойных связей. Жирные кислоты можно условно поделить на низшие (до семи атомов углерода), средние (восемь — двенадцать атомов углерода) и высшие (более двенадцати атомов углерода). Исходя из исторического названия данные вещества должны быть компонентами жиров. На сегодня это не так; термин «жирные кислоты» подразумевает под собой более широкую группу веществ.
Карбоновые кислоты начиная с масляной кислоты (С4) считаются жирными, в то время как жирные кислоты, полученные непосредственно из животных жиров, имеют в основном восемь и больше атомов углерода (каприловая кислота). Число атомов углерода в натуральных жирных кислотах в основном чётное, что обусловлено их биосинтезом с участием ацетил-кофермента А.
Большая группа жирных кислот (более 400 различных структур, хотя только 10—12 распространены) находятся в растительных маслах семян. Наблюдается высокое процентное содержание редких жирных кислот в семенах определённых семейств растений.
Под незаменимыми понимаются те жирные кислоты, которые не могут быть синтезированы в организме. Для человека незаменимыми являются кислоты, содержащие по крайней мере одну двойную связь на расстоянии более девяти атомов углерода от карбоксильной группы.
Биохимия
Расщепление
Жирные кислоты в виде триглицеридов накапливаются в жировых тканях. При потребности под действием таких веществ как адреналин, норадреналин, глюкагон и адренокортикотропина запускается процесс липолиза. Освобождённые жирные кислоты выделяются в кровоток, по которому попадают к нуждающимся в энергии клеткам, где сперва при участии АТФ происходит связывание (активация) с коферментом А (КоА). При этом АТФ гидролизуется до АМФ с освобождением двух молекул неорганического фосфата (Pi).
- R-COOH + КоА-SH + АТФ → R-CO-S-КоА + 2Pi + H+ + АМФ
Синтез
В растительном и животном организме жирные кислоты образуются, как продукты углеводного и жирового обмена. Синтез жирных кислот осуществляется в противоположность расщеплению в цитозоле.
Циркуляция
Пищеварение и всасывание
Коротко- и среднецепочечные жирные кислоты всасываются напрямую в кровь через капилляры кишечного тракта и проходят через воротную вену, как и другие питательные вещества. Более длинноцепочечные слишком велики, чтобы проникнуть напрямую через маленькие капилляры кишечника. Вместо этого они поглощаются жирными стенками ворсинок кишечника и заново синтезируются в триглицериды. Триглицериды покрываются холестерином и белками с образованием хиломикрона. Внутри ворсинки хиломикрон попадает в лимфатические сосуды, так называемый млечный капилляр, где поглощается большими лимфатическими сосудами. Он транспортируется по лимфатической системе вплоть до места, близкого к сердцу, где кровеносные артерии и вены наибольшие. Грудной канал освобождает хиломикрон в кровоток посредством подключичной вены. Таким образом триглицериды транспортируются в места, где в них нуждаются. [2]
Виды существования в организме
Жирные кислоты существуют в различных формах на различных стадиях циркуляции в крови. Они поглощаются в кишечнике, образуя хиломикроны, но в то же время они существуют в виде липопротеинов очень низкой плотности или липопротеинов низкой плотности после превращений в печени. При выделении из адипоцитов жирные кислоты поступают в свободном виде в кровь.
Кислотность
Кислоты с коротким углеводородным хвостом, такие как муравьиная и уксусная кислоты, полностью смешиваются с водой и диссоциируют с образованием достаточно кислых растворов (pKa 3.77 и 4.76, соответственно). Жирные кислоты с более длинным хвостом незначительно отличаются по кислотности. Например, нонановая кислота имеет pKa 4.96. Однако с увеличением длины хвоста растворимость жирных кислот в воде уменьшается очень быстро, в результате чего эти кислоты мало изменяют pH раствора. Значение величин pKa для данных кислот приобретает значение лишь в реакциях, в которые эти кислоты способны вступить. Кислоты, нерастворимые в воде, могут быть растворены в тёплом этаноле, и оттитрованы раствором гидроксида натрия, используя фенолфталеин, в качестве индикатора до бледнорозового цвета. Такой анализ позволяет определить содержание жирных кислот в порции триглицеридов после гидролиза.
Реакции жирных кислот
Жирные кислоты реагируют так же, как и другие карбоновые кислоты, что подразумевает этерификацию и кислотные реакции. Восстановление жирных кислот приводит к жирным спиртам. Ненасыщенные жирные кислоты также могут вступать в реакции присоединения; наиболее характерно гидрирование, которое используется для превращения растительных жиров в маргарин. В результате частичного гидрирования ненасыщенных жирных кислот цис-изомеры, характерные для природных жиров, могут перейти в транс-форму. В реакции Варрентраппа ненасыщенные жиры могут быть расщеплены в расплавленной щёлочи. Эта реакция имеет значение для определения структуры ненасыщенных жирных кислот.
Автоокисление и прогоркание
Жирные кислоты при комнатной температуре подвергаются автоокислению и прогорканию. При этом они разлагаются на углеводороды, кетоны, альдегиды и небольшое количество эпоксидов и спиртов. Тяжёлые металлы, содержащиеся в небольших количествах в жирах и маслах, ускоряют автоокисление. Чтобы избежать этого, жиры и масла часто обрабатываются хелатирующими агентами, такими как лимонная кислота.
Применение
Натриевые и калиевые соли высших жирных кислот являются эффективными ПАВ и используются в качестве мыл. В пищевой промышленности жирные кислоты зарегистрированы в качестве пищевой добавки E570, как стабилизатор пены, глазирователь и пеногаситель. [1]
Разветвлённые жирные кислоты
Разветвлённые карбоновые кислоты липидов обычно не относятся к собственно жирным кислотам, но рассматриваются как их метилированные производные. Метилированные по предпоследнему атому углерода (изо-жирные кислоты) и по третьему от конца цепи (антеизо-жирные кислоты) входят в качестве минорных компонент в состав липидов бактерий и животных.
Разветвленные карбоновые кислоты также входят в состав эфирных масел некоторых растений: так, например, в эфирном масле валерианы содержится изовалериановая кислота:
Основные жирные кислоты
Насыщенные жирные кислоты
Общая формула: CnH2n+1COOH или CH3-(CH2)n-COOH
| Тривиальное название | Систематическое название (IUPAC) | Брутто формула | Рациональная полуразвернутая формула | Нахождение | Т.пл. | pKa |
|---|---|---|---|---|---|---|
| Масляная кислота | Бутановая кислота | C3H7COOH | CH3(CH2)2COOH | Сливочное масло, древесный уксус | −8 °C | 4,82 |
| Капроновая кислота | Гексановая кислота | C5H11COOH | CH3(CH2)4COOH | Нефть | −4 °C | 4,85 |
| Каприловая кислота | Октановая кислота | C7H15COOH | CH3(CH2)6COOH | 17 °C | 4,89 | |
| Пеларгоновая кислота | Нонановая кислота | C8H17COOH | CH3(CH2)7COOH | 12,5 °C | 4.96 | |
| Каприновая кислота | Декановая кислота | C9H19COOH | CH3(CH2)8COOH | Кокосовое масло | 31 °C | |
| Лауриновая кислота | Додекановая кислота | С11Н23СООН | CH3(CH2)10COOH | 43,2 °C | ||
| Миристиновая кислота | Тетрадекановая кислота | С13Н27СООН | CH3(CH2)12COOH | 53,9 °C | ||
| Пальмитиновая кислота | Гексадекановая кислота | С15Н31СООН | CH3(CH2)14COOH | 62,8 °C | ||
| Маргариновая кислота | Гептадекановая кислота | С16Н33СООН | CH3(CH2)15COOH | 61,3 °C | ||
| Стеариновая кислота | Октадекановая кислота | С17Н35СООН | CH3(CH2)16COOH | 69,6 °C | ||
| Арахиновая кислота | Эйкозановая кислота | С19Н39СООН | CH3(CH2)18COOH | 75,4 °C | ||
| Бегеновая кислота | Докозановая кислота | С21Н43СООН | CH3(CH2)20COOH | |||
| Лигноцериновая кислота | Тетракозановая кислота | С23Н47СООН | CH3(CH2)22COOH | |||
| Церотиновая кислота | Гексакозановая кислота | С25Н51СООН | CH3(CH2)24COOH | |||
| Монтановая кислота | Октакозановая кислота | С27Н55СООН | CH3(CH2)26COOH |
Мононенасыщенные жирные кислоты
Общая формула: СН3-(СН2)m-CH=CH-(CH2)n-COOH (m=ω-2; n=Δ-2)
| Тривиальное название | Систематическое название (IUPAC) | Брутто формула | IUPAC формула (с метил.конца) | IUPAC формула (с карб.конца) | Рациональная полуразвернутая формула | |
|---|---|---|---|---|---|---|
| Акриловая кислота | 2-пропеновая кислота | С2Н3COOH | 3:1ω1 | 3:1Δ2 | СН2=СН-СООН | |
| Метакриловая кислота | 2-метил-2-пропеновая кислота | С3Н5OOH | 4:1ω1 | 3:1Δ2 | СН2=С(СН3)-СООН | |
| Кротоновая кислота | 2-бутеновая кислота | С3Н5СOOH | 4:1ω2 | 4:1Δ2 | СН2-СН=СН-СООН | |
| Винилуксусная кислота | 3-бутеновая кислота | С3Н6СOOH | 4:1ω1 | 4:1Δ3 | СН2=СН-СН2-СООН | |
| Лауроолеиновая кислота | цис-9-додеценовая кислота | С11Н21СOOH | 12:1ω3 | 12:1Δ9 | СН3-СН2-СН=СН-(СН2)7-СООН | |
| Миристоолеиновая кислота | цис-9-тетрадеценовая кислота | С13Н25СOOH | 14:1ω5 | 14:1Δ9 | СН3-(СН2)3-СН=СН-(СН2)7-СООН | |
| Пальмитолеиновая кислота | цис-9-гексадеценовая кислота | С15Н29СOOH | 16:1ω7 | 16:1Δ9 | СН3-(СН2)5-СН=СН-(СН2)7-СООН | |
| Петроселиновая кислота | цис-6-октадеценовая кислота | С17Н33СOOH | 18:1ω12 | 18:1Δ6 | СН3-(СН2)16-СН=СН-(СН2)4-СООН | |
| Олеиновая кислота | цис-9-октадеценовая кислота | С17Н33СOOH | 18:1ω9 | 18:1Δ9 | СН3-(СН2)7-СН=СН-(СН2)7-СООН | |
| Элаидиновая кислота | транс-9-октадеценовая кислота | С17Н33СOOH | 18:1ω9 | 18:1Δ9 | СН3-(СН2)7-СН=СН-(СН2)7-СООН | |
| Цис-вакценовая кислота | цис-11-октадеценовая кислота | С17Н33СOOH | 18:1ω7 | 18:1Δ11 | СН3-(СН2)5-СН=СН-(СН2)9-СООН | |
| Транс-вакценовая кислота | транс-11-октадеценовая кислота | С17Н33СOOH | 18:1ω7 | 18:1Δ11 | СН3-(СН2)5-СН=СН-(СН2)9-СООН | |
| Гадолеиновая кислота | цис-9-эйкозеновая кислота | С19Н37СOOH | 20:1ω11 | 19:1Δ9 | СН3-(СН2)9-СН=СН-(СН2)7-СООН | |
| Гондоиновая кислота | цис-11-эйкозеновая кислота | С19Н37СOOH | 20:1ω9 | 20:1Δ11 | СН3-(СН2)7-СН=СН-(СН2)9-СООН | |
| Эруковая кислота | цис-9-доказеновая кислота | С21Н41СOOH | 22:1ω13 | 22:1Δ9 | СН3-(СН2)11-СН=СН-(СН2)7-СООН | |
| Нервоновая кислота | цис-15-тетракозеновая кислота | С23Н45СOOH | 24:1ω9 | 23:1Δ15 | СН3-(СН2)7-СН=СН-(СН2)13-СООН |
Полиненасыщенные жирные кислоты
Общая формула: СН3-(СН2)m-(CH=CH-(CH2)х(СН2)n-COOH
| Тривиальное название | Систематическое название (IUPAC) | Брутто формула | IUPAC формула (с метил.конца) | IUPAC формула (с карб.конца) | Рациональная полуразвернутая формула | |
|---|---|---|---|---|---|---|
| Сорбиновая кислота | транс,транс-2,4-гексадиеновая кислота | С5Н7COOH | 6:2ω3 | 6:2Δ2,4 | СН3-СН=СН-СН=СН-СООН | |
| Линолевая кислота | цис,цис-9,12-октадекадиеновая кислота | С17Н31COOH | 18:2ω6 | 18:2Δ9,12 | СН3(СН2)3-(СН2-СН=СН)2-(СН2)7-СООН | |
| Линоленовая кислота | цис,цис,цис-6,9,12-октадекатриеновая кислота | С17Н28COOH | 18:3ω6 | 18:3Δ6,9,12 | СН3-(СН2)-(СН2-СН=СН)3-(СН2)6-СООН | |
| Линоленовая кислота | цис,цис,цис-9,12,15-октадекатриеновая кислота | С17Н29COOH | 18:3ω3 | 18:3Δ9,12,15 | СН3-(СН2-СН=СН)3-(СН2)7-СООН | |
| Арахидоновая кислота | цис-5,8,11,14-эйкозотетраеновая кислота | С19Н31COOH | 20:4ω6 | 20:4Δ5,8,11,14 | СН3-(СН2)4-(СН=СН-СН2)4-(СН2)2-СООН | |
| Дигомо-γ-линоленовая кислота | 8,11,14-эйкозатриеновая кислота | С19Н33COOH | 20:3ω6 | 20:3Δ8,11,14 | СН3-(СН2)4-(СН=СН-СН2)3-(СН2)5-СООН | |
| — | 4,7,10,13,16-докозапентаеновая кислота | С19Н29COOH | 20:5ω4 | 20:5Δ4,7,10,13,16 | СН3-(СН2)2-(СН=СН-СН2)5-(СН2)-СООН | |
| Тимнодоновая кислота | 5,8,11,14,17-эйкозапентаеновая кислота | С19Н29COOH | 20:5ω3 | 20:5Δ5,8,11,14,17 | СН3-(СН2)-(СН=СН-СН2)5-(СН2)2-СООН | |
| Цервоновая кислота | 4,7,10,13,16,19-докозагексаеновая кислота | С21Н31COOH | 22:6ω3 | 22:3Δ4,7,10,13,16,19 | СН3-(СН2)-(СН=СН-СН2)6-(СН2)-СООН | |
| — | 5,8,11-эйкозатриеновая кислота | С19Н33COOH | 20:3ω9 | 20:3Δ5,8,11 | СН3-(СН2)7-(СН=СН-СН2)3-(СН2)2-СООН |
Примечания
См. также
 |
 |
Карбоновые кислоты.
Органическая химия
Карбоновые кислоты.
Строение карбоновых кислот
Карбоновые кислоты — это органические соединения, которые характеризуются присутствием в их молекулах карбоксильной группы -СООН.
Карбоксильная группа является функциональной (характеристической) группой этого класса соединений. Примерами карбоновых кислот могут служить:
Свойства карбоновых кислот.
Кислотный характер этих соединений является результатом того, что атом водорода гидроксильной группы способен диссоциировать с образованием иона водорода, например:
Взаимодействуя с основаниями карбоновые кислоты образуют соли:
Карбоновые кислоты являются слабыми кислотами, поэтому их соли подвергаются обратимоми гидролизу. Наиболее сильные из карбоновых кислот – муравьиная и уксусная.
Карбоновые кислоты со спиртами образуют сложные эфиры. Сложные эфиры – чрезвычайно важное соединение, очень часто встречающееся в продуктах животного и растительного мира.
Классификация карбоновых кислот.
Карбоновые кислоты можно классифицировать по различным признакам:
- По количеству гидрокильных групп (одно- и двухосновные),
- По числу атомов углерода (низшие, средние, высшие),
- По наличию в них предельных и не предельных связей (предельные и непредельные).
Одноосновные и двухосновные карбоновые кислоты.
Карбоновые кислоты делятся одноосновные и двухосновные в зависимости от кличества в их составе гидроксильных групп ОН.
Все карбоновые кислоты, рассмотренные выше – это примеры одноосновных кислот. В их сотавах содержится по одной гидроксильной группе.
Соответственно, в молекулах двухосновных кислот содержится по две гидроксильных группы. К двухосновным карбоновым кислотам относятся, например, щавелевая или терефталиевая кислоты.
Низшие, средние и высшие карбоновые кислоты.
По числу атомов углерода в молекуле карбоновые кислоты делят на:
Низшие (С1-С3),
Средние (С4-С8) и
Высшие (С9-С26).
Высшие карбоновые кислоты называют высшими жирными кислотами, по причине того, что они входят в состав природных жиров.
Но иногда жирными называют все ациклические карбоновые кислоты. Таким образом, термины «жирные кислоты» и «карбоновые кислоты» часто используются как синонимы.
Предельные и непредельные карбоновые кислоты.
Предельные карбоновые кислоты в своём составе, содержат радикал предельных углеводородов, т.е. радикал только с простыми, одинарными связями.
И наоборот, непредельные карбоновые кислоты в своём составе содержат радикал непредельных углеводородов, т.е. радикал, в котором присутствуют кратные (двойные и тройные) связи.
Высшие карбоновые (жирные) кислоты
Напомним, что высшим карбоновым кислотам относят такие карбоновые кислоты, молекулы которых содержат сравнительно большое число атомов углерода (С9-С26).
По причине того, что высшие карбоновые кислоты входят в состав животных и растительных жиров их называют высшими жирными кислотами.
Примеры предельных высших жирных кислот:
- Каприновая кислота — C9H19COOH,
- Лауриновая кислота — С11Н23СООН,
- Миристиновая кислота — С13Н27СООН,
- Пальмитиновая кислота — С15Н31СООН,
- Стеариновая кислота – С17Н35СООН.
Примеры непредельных высших жирных кислот:
- Олеиновая кислота — С17Н33СООН – имеет одну двойную связь,
- Линолевая кислота – С17Н31СООН — имеет две двойных связи,
- Линоленовая кислота – С17Н29СООН – имеет три двойных связи.
Структурные формулы соединений, в которых присутствуют длинные углеводородный радикалы, часто изображают следующим образом:
В углеводородной цепи атомы углерода расположены не по прямой линии, а виде «змейки». Угол между двумя соседними отрезками такой «змейки» 109 градусов 28 минут. В случае двойной связи угол другой. В структурной формуле каждая вершина такой «змейки» означает атом углерода, соединённый с двумя атомами водорода. Последний атом углерода соединён с тремя атомами водорода. При этом сами символы углерода (С) и водорода(Н) не изображаются.
Предельные и непредельные жирные кислоты имеют в значительной степени различные свойства.
Высшие предельные кислоты – воскообразные вещества, непредельные – жидкости (напоминающие растительное масло).
Натриевые и калиевые соли высших жирных кислот называют мылами.
Например:
C17H35COONa – стеарат натрия,
СН31СООК – пальмитат калия.
Натриевые мыла – твёрдые, калиевые – жидкие.
Примеры карбоновых кислот
Уксусная кислота
Уксусная кислота – жилкость с острым раздражающим запахом.
Температура кипения 118,5 градусов С, при +16,6 градусах С застывает в кристаллическую массу, похожую на лёд.
Смешивается с водой в любых соотношениях.
Широко применяется как прправа к пище и консервирующее средство. В продаже встречается в виде уксусной эссенции (80%) и уксуса (9,3%).
Натуральный или винный уксус – продукт, содержащий уксусную кислоту и получающийся при скисании виноградного вина.
Уксусная кислота используется также при синтезе многих органических веществ и в качестве растворителя.
Уксусную кислоту получают преимущественно синтезом из ацетилена – присоединением к нему воды и окислением образующегося уксусного альдегида.
Бензойная кислота
Бензойная кислота простейшая одноосновная кислота ароматического ряда. Формула С6Н5-СООН.
На вид – бесцветные кристаллы.
Бензойная кислота – антисептик. Применяется для консервирования пищевых продуктови во многих органических синтезах.
Щавелевая кислота
Щавелевая кислота – простейшая двухосновная карбоновая кислота.
Формула НООС-СООН.
Щавелевая кислота – кристаллическое вещество, растворяется в воде, ядовита.
В виде кислой калиевой соли содержится во многих растениях.
Применяется для крашения тканей.
Терефталевая кислота
Терефталевая кислота НООС-С6Н4-СООН
Двухосновная карбоновая кислота ароматического ядра.
Её структурная формула:
Из терефталевой кислоты и этиленгликоля получают синтетическое волокно лавсан.
Молочная кислота
Молочная кислота может служить примером соединения со смешанными функциями – проявляет свойства кислоты и спирта (спиртокислота)
Она образуется при молочнокислом брожении сахаристых веществ, вызываемых особыми бактериями. Содержится в кислом молоке, рассоле квашеной капусты, силосе.
Салициловая кислота
Салициловая кислота – аналог молочной кислоты в ароматическом ряду. Имеет строение:
Относится к соединениям со смешанными функциями – проявляет свойства кислоты и фенола (фенолокислота).
Салициловая кислота – антисептик. Её используют (особенно её соли и эфиры) как лекарственное вещество.
Также салициловую кислоту используют при синтезе других продуктов.
Жиры, подготовка к ЕГЭ по химии
Жиры — органические соединения, по строению являющиеся сложными эфирами трехатомного спирта глицерина и высших карбоновых (жирных) кислот.
К жирным кислотам (их формулы лучше выучить 😉 относятся:
- Пальмитиновая — C15H31COOH (предельная)
- Стеариновая — C17H35COOH (предельная)
- Олеиновая — C17H33COOH (непредельная, 1 двойная связь в радикале)
- Линолевая — C17H31COOH (непредельная, 2 двойные связи в радикале)
- Линоленовая — C17H29COOH (непредельная, 3 двойные связи в радикале)
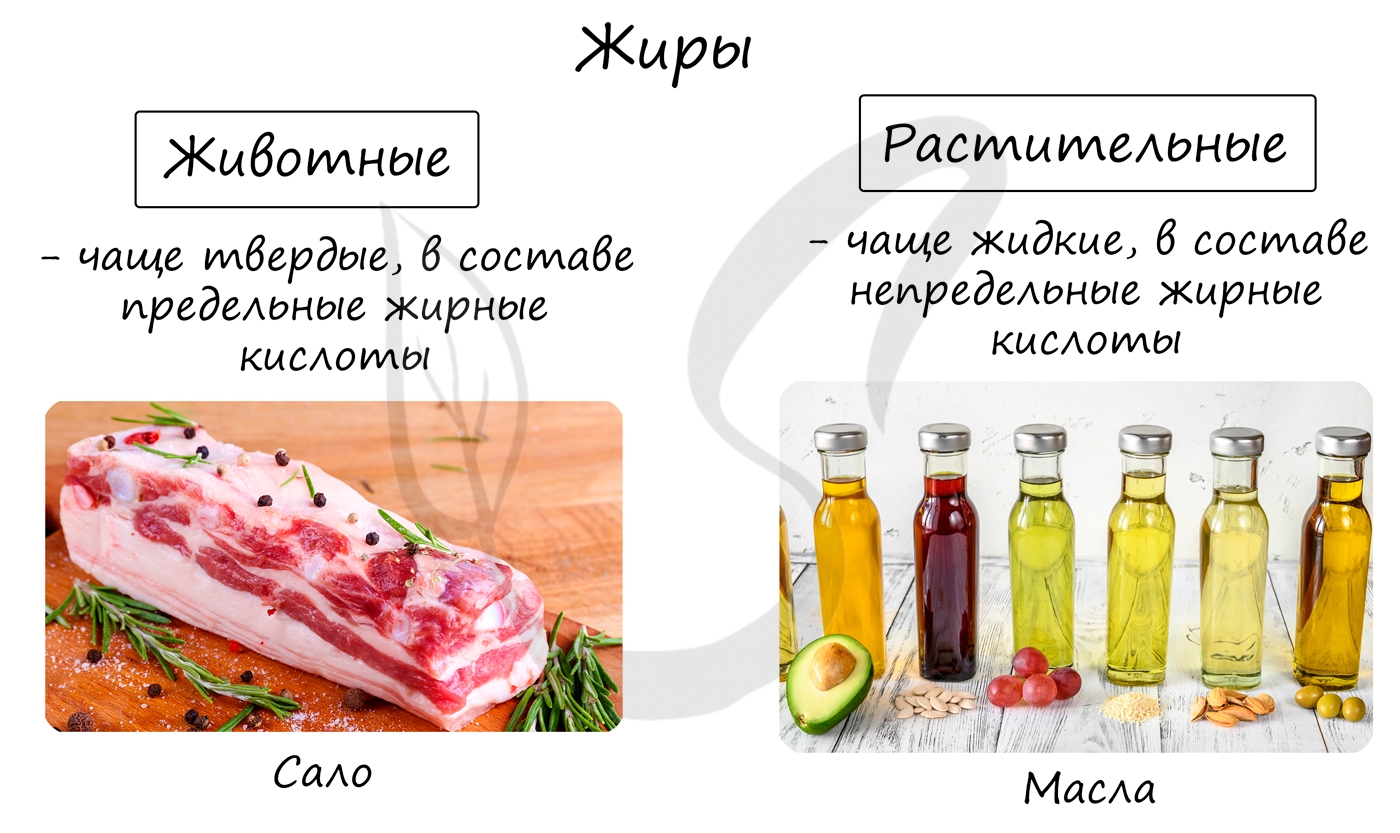
Растительные и животные жиры
Жиры образуются в организме растений и животных, служат запасным питательным веществом. В строении растительных и животных жиров есть некоторые важные отличия.
Заметьте, что растительные жиры чаще жидкие и в них входят преимущественно остатки непредельных жирных кислот, а животные жиры — твердые и содержат остатки предельных жирных кислот.
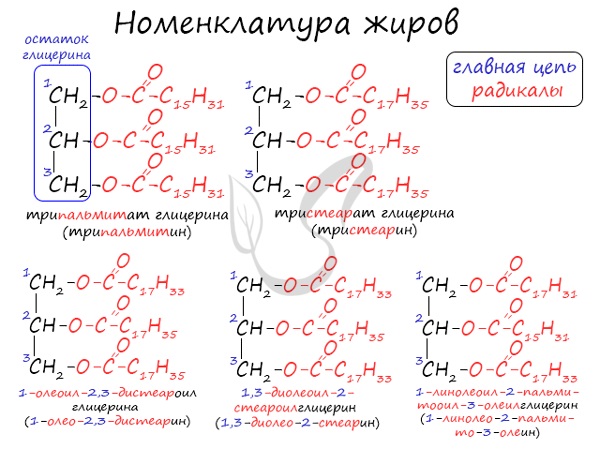
Номенклатура жиров
По систематической номенклатуре жиры принято называть триацилглицеринами. Названия жирам дают в зависимости от ацилов — остатков жирных кислот, входящих в их состав. Для формирования единого названия к остаткам кислот добавляют суффикс «оил».
В соответствии с тривиальной номенклатурой, жиры называют, добавляя окончание «ин» к названию кислоты и приставку, указывая, сколько гидроксогрупп в молекуле глицерина подверглось этерификации. В общем лучше 1 раз увидеть, чем 100 раз услышать ;)
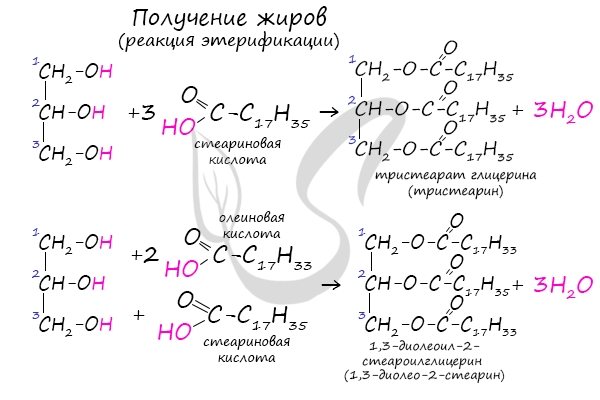
Получение жиров
Жиры (по строению сложные эфиры) получаются в реакции этерификации, протекающей между трехатомным спиртом глицерином и высшими карбоновыми (жирными) кислотами.
В зависимости от того, какие именно кислоты участвуют в реакции, образуются различные жиры.
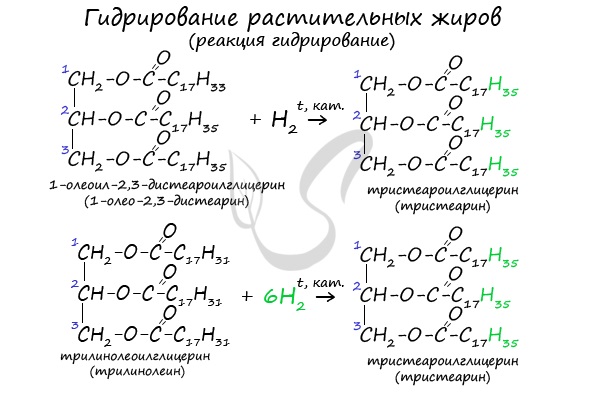
Химические свойства жиров
- Гидрирование растительных жиров
- Гидролиз
В состав растительных жиров входят непредельные кислоты, которые поддаются гидрированию и превращаются в предельные. Таким путем в пищевой промышленности получают маргарин.
Как сложные эфиры, жиры способны вступать в реакцию гидролиза, который может быть кислотным и щелочным. В результате кислотного гидролиза образуется глицерин и исходные жирные кислоты, в результате щелочного гидролиза — глицерин и соли жирных кислот.
Реакция щелочного гидролиза жиров называется реакцией омыления, в результате получаются соли жирных кислот — мыла. Кислотный гидролиз протекает обратимо, щелочной — необратимо.
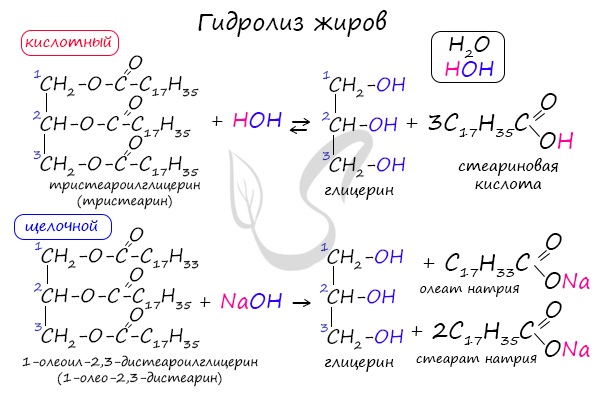
В состав твердого мыла входят соли Na, в состав жидкого — K.
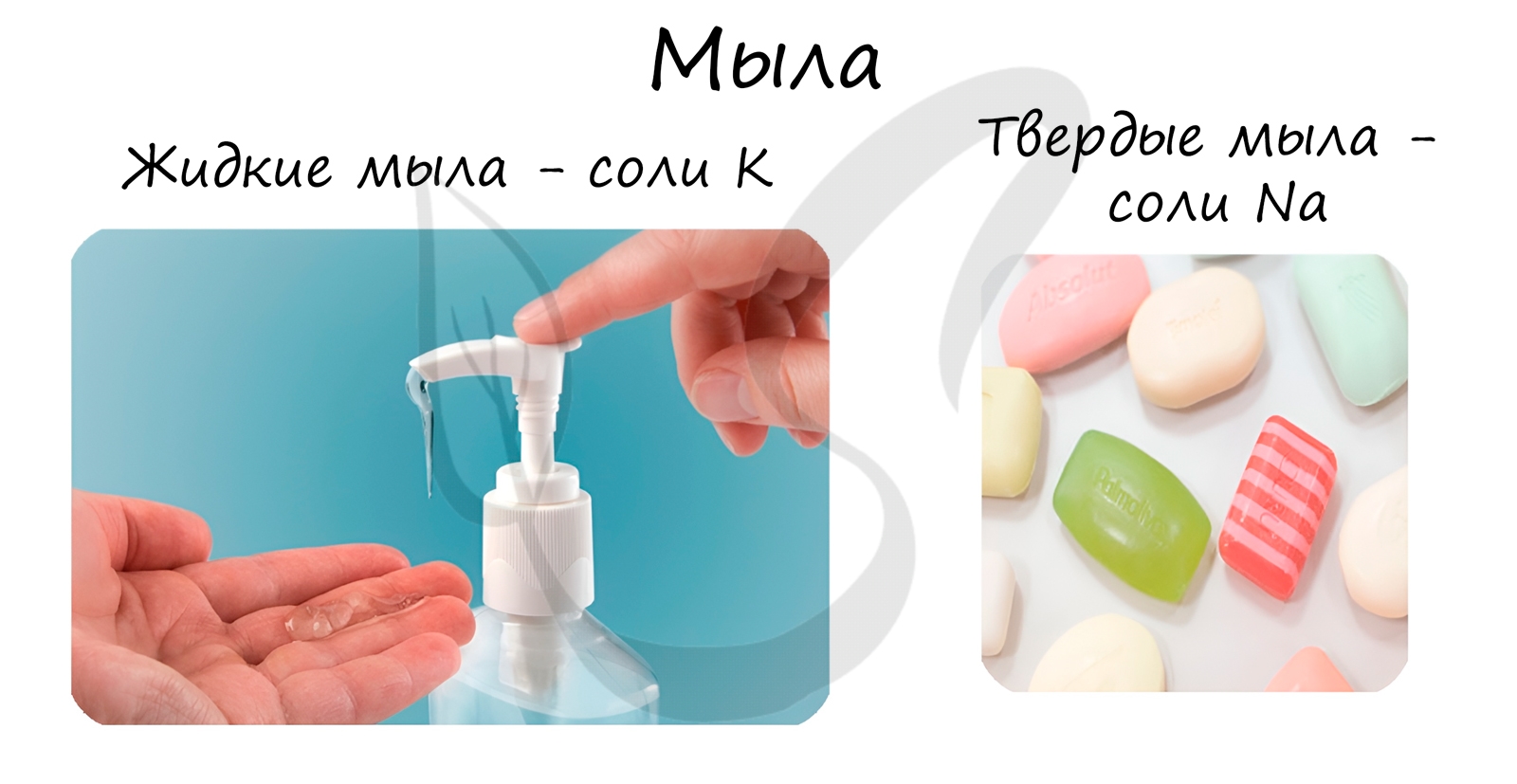
©Беллевич Юрий Сергеевич
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Предельные одноосновные кислоты жирного ряда
Органические кислоты, кислотные свойства которых связаны с присутствием в молекуле одновалентного радикала карбоксила
называются карбоновыми кислотами. По числу карбоксилов в молекуле различают кислоты одноосновные, двухосновные и многоосновные.
Предельные жирные кислоты можно рассматривать как производные парафиновых углеводородов, происшедшие в результате замещения атома водорода на карбоксил. Таким образом, общая формула этих кислот Cn’H2n’+1—СООН, или CnH2nO2 (принимая п = п’ + 1). Следовательно, число изомеров жирных кислот (как и альдегидов) будет совпадать с числом изомеров, например, галоидных соединений и спиртов, содержащих в молекуле на один атом углерода меньше, чем кислота.
Если производить кислоты от парафиновых углеводородов, то первым членом этого ряда являлась бы кислота строения СН3—СООН, т. е. метанкарбоновая, или уксусная, кислота. Однако аналогично некоторым другим случаям в качестве первого члена этого ряда рассматривают муравьиную кислоту Н—СООН, представляющую собой соединение карбоксила с водородом.
Высшие кислоты можно также рассматривать как производные уксусной кислоты — продукты замещения атомов водорода в метиле на алкильные группы. Тогда пропионовую, или этанкарбоновую, кислоту СН3—СН2—СООН можно назвать метилуксусной кислотой, изомасляную (СН3)2СН—СООН — диметилуксусной кислотой и т. д.
По женевской номенклатуре, названия кислот производятся от названий углеводородов с тем же числом атомов углерода, с прибавлением слова кислота, обозначающего наличие в молекуле карбоксила. Таким образом, муравьиная кислота называется метановой кислотой, уксусная — этановой кислотой, кислота строения
3-метилбутановой кислотой и т. д.
Наиболее употребительными являются более или менее случайные названия кислот, связанные с каким-либо из источников их получения или с местонахождением в природе; эти названия приведены в табл. 10.
При действии щелочей карбоновые кислоты образуют соли, причем экспериментально установлено, что в карбоксильной группе соли, как и в карбоксильной группе кислоты, оба кислородных атома равноценны; так, например, в формиате натрия угол между связями О—С—О равен 124 ±4°, а оба расстояния С—О равны и составляют 1,27 Å. Поэтому строение солей карбоновых кислот может быть изображено формулой:
(кривыми стрелками показано направление смещения электронной плотности в результате взаимного влияния атомов).