Глюкоза — Википедия
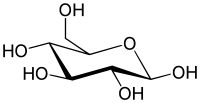
| Глюкоза[1] | |
|---|---|
 | |
| Систематическое наименование | (2R,3S,4R,5R)-2,3,4,5,6-пентагидроксигексаналь (D-глюкоза), (2S,3R,4S,5S)-2,3,4,5,6-пентагидроксигексаналь (L-глюкоза) |
| Традиционные названия | Глюкоза, декстроза |
| Хим. формула | C6H12O6 |
| Состояние | бесцветные кристаллы |
| Молярная масса | 180,16 г/моль |
| Плотность | 1,5620 г/см³ |
| Температура | |
| • плавления | α-D-глюкоза: 146 °C (моногидрат: 83 °C) β- |
| Растворимость | |
| • в воде | 82 г/100 мл |
| • в 80 % этаноле | 2 г/100 мл |
| Вращение [α]D{\displaystyle [\alpha ]_{D}} | α-D-глюкоза: +112,2° β-D-глюкоза: +18,7° |
| Дипольный момент | 14,1 Д |
| Рег. номер CAS | 50-99-7 (D-глюкоза) 921-60-8 (L-глюкоза) |
| PubChem | 24895228 |
| Рег. номер EINECS | 200-075-1 |
| SMILES | |
| InChI | |
| RTECS | LZ6600000 |
| ChEBI | 17234 |
| NFPA 704 |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
Глюко́за, или виноградный сахар, или декстроза (D-глюкоза), C6H12O6 — органическое соединение, моносахарид (шестиатомный гидроксиальдегид, гексоза), один из самых распространённых источников энергии в живых организмах на планете[2]. Встречается в соке многих фруктов и ягод, в том числе и винограда, от чего и произошло название этого вида сахара. Глюкозное звено входит в состав полисахаридов (целлюлоза, крахмал, гликоген) и ряда дисахаридов (мальтозы, лактозы и сахарозы), которые, например, в пищеварительном тракте быстро расщепляются на глюкозу и фруктозу.
Вероятно, глюкоза известна человеку с древних времён, поскольку она кристаллизуется из мёда. Однако в чистом виде её выделили гораздо позже: немецкий химик Андреас Маргграф получил её в 1747 году из виноградного сока. Жозеф Луи Пруст в 1801 году осадил кристаллы α-
Использование глюкозы в качестве подсластителя связано с тем, что во время Наполеоновских войн были заблокированы поставки тростникового сахара из Вест-Индии. Ещё в 1000 году до н. э. в Китае из крахмала (ферментацией риса) получали искусственный подсластитель — дисахарид мальтозу. К концу XVIII в. в Европе было известно, что крахмал можно обработать кислотой и получить сладкое вещество. Именно это позволило К. С. Кирхгофу нагреванием картофельного крахмала с серной кислотой получить сладкое сиропообразное вещество. В результате оптимизации процесса он получил сироп, который кристаллизовался при стоянии. Кроме того, была предпринята попытка прессовать получаемую массу в твёрдый продукт и в таком виде продавать. Однако организовать производство не удалось, поскольку Наполеон потерпел поражение и поставки сахара были восстановлены [3].
Процесс получения глюкозы исследовал французский химик Соссюр. Он выяснил, что крахмал подвергается гидролизу, при котором разрушаются связи между углеводными фрагментами, причём на каждый разрыв расходуется по одной молекуле воды. Также было обнаружено, что конфеты, производимые из сиропов глюкозы, не такие сладкие, как те, что получают из сахарозы. Поэтому в Германии и других странах Европы было организовано производство глюкозы[3].
В то время промышленная глюкоза была недостаточно чистой и получалась в виде сиропов. Её приходилось многократно кристаллизовать из воды или использовать органические растворители. Единственной твёрдой формой, которую выпускали в большом количестве, была литая глюкоза: сироп заливали в формы, где он затвердевал
В 1923 году в США Уильям Б. Ньюкирк (англ. William B. Newkirk) запатентовал промышленный способ получения глюкозы. Этот способ отличался тщательным контролем условий кристаллизации, благодаря чему глюкоза выпадала из раствора в виде чистых, крупных кристаллов[3].
Глюкоза принадлежит к классу альдогексоз, то есть является полигидроксиальдегидом, содержащим шесть атомов углерода, альдегидную группу и пять гидроксильных групп. Четыре атома углерода в её структуре являются хиральными, поэтому существует 16 стереоизомерных альдогексоз: некоторые встречаются в природе, некоторые получены синтетически. Конкретную конфигурацию хиральных центров глюкозы в конце XIX в. установил немецкий химик Эмиль Фишер. Он сделал это при помощи реакций наращивания и деградации углеродной цепи сахаров. Наряду с наиболее распространённым в природе моносахаридом D-глюкозой существует также её энантиомер L-глюкоза,который в природе практически не встречается [4][5].
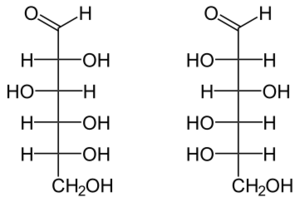 D-глюкоза (слева) и L-глюкоза (справа)
D-глюкоза (слева) и L-глюкоза (справа)Часто D-глюкозу изображают в линейной форме, однако в действительности D-глюкоза существует в циклической форме, образованной в результате присоединения ОН-группы при углероде С-5 к альдегидной группе. Образующийся при этом циклический полуацеталь устойчив: в растворах и кристаллической форме D-глюкоза более чем на 99 % находится в форме полуацеталя. В общем такую форму называют пиранозной (от названия пирана — шестичленного гетероцикла с одним атомом кислорода), а циклическую D-глюкозу называют D-глюкопиранозой[6].
При описанной циклизации возникает новый стереоцентр при полуацетальном атоме углерода, поэтому D-глюкопираноза может существовать в виде двух диастереомеров, называемых аномерами: α-D-глюкопиранозы и β-D-глюкопиранозы (или кратко: α-D-глюкозы и β-D-глюкозы; α-аномера и β-аномера). Изображать циклические формы углеводов удобно при помощи проекций Хеуорса — идеализированных шестичленных циклов с заместителями над и под плоскостью цикла
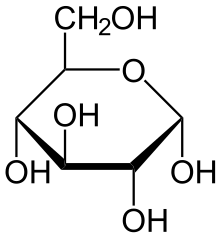 α-D-Глюкопираноза α-D-Глюкопираноза | 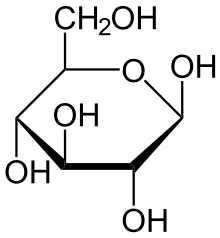 β-D-Глюкопираноза β-D-Глюкопираноза |
Наиболее близко к истине структуру молекулы глюкозы можно изобразить, используя конформацию «кресло». В таком представлении все гидроксильные группы D-глюкопиранозы находятся в экваториальных положениях (кроме аномерной, которая может находиться в экваториальном либо аксиальном положении в зависимости от аномера). Экваториальные положения более выгодны по сравнению с аксиальными: это объясняет, почему глюкоза является наиболее распространённым моносахаридом [6].
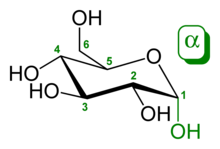 α-D-Глюкопираноза α-D-Глюкопираноза |  β-D-Глюкопираноза β-D-Глюкопираноза |
В растворах α-D-глюкопираноза и β-D-глюкопираноза существуют в равновесии и взаимопревращаются через образование открытоцепной формы. Равновесная доля α-аномера при 31 °С составляет 38 %, а более устойчивого β-аномера — 62 %[7]. Чистые аномеры можно получить в кристаллическом виде: α-аномер кристаллизуется из воды в виде моногидрата, а β-аномер кристаллизуется из пиридина
Глюкоза — бесцветное кристаллическое вещество без запаха. Обладает сладким вкусом. D-глюкоза представлена в виде трёх кристаллических форм: безводной α-D-глюкопиранозы, моногидрата α-D-глюкопиранозы и безводной β-D-глюкопиранозы (хотя описан также моногидрат β-D-глюкопиранозы). Безводные формы имеют орторомбические кристаллы, а гидрат — моноклинные[7]. Все три формы отличаются температурой плавления: α-аномер плавится при 146 °С, его моногидрат — при 83 °С, β-аномер — при 148–150 °С[8].
Аномеры D-глюкопиранозы оптически активны: удельное вращение α-аномера составляет +112,2°, β-аномера — +18,9°[8]. Оба аномера при растворении претерпевают мутаротацию, то есть превращаются в равновесную смесь, состоящую из 62 % β-аномера и 38 % α-аномера[7]. Удельное вращение этой смеси составляет +52,7°[8].
Производство глюкозных сиропов[править | править код]
Кислотный гидролиз крахмала[править | править код]
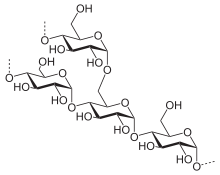
Единственным сырьём для производства глюкозы является крахмал, хотя делаются попытки использовать другой природный полимер глюкозы — целлюлозу. Основным источником крахмала является кукуруза: 100 % глюкозных подсластителей в США и 84 % в Японии производят из кукурузного крахмала. Также 70 % производимой в мире кукурузы идёт на производство глюкозы. В Европе постепенно возрастает использование пшеничного крахмала, хотя в основном используется также кукурузный крахмал. В Австралии глюкозу получают только из пшеничного крахмала. В Азии используют крахмал из саго, тапиоки и кукурузы[9].
Для получения глюкозы крахмал гидролизуют в присутствии кислот или ферментов. При этом происходит разрыв связей между глюкозными звеньями полимерных амилозы и амилопектина — компонентов крахмала — и образуется мономер (D-глюкоза) с некоторым содержанием димеров: мальтозы и изомальтозы. Для кислотного гидролиза готовят суспензию крахмала в воде (30-40 мас. %) и доводят pH до 2 или ниже. При атмосферном давлении кислотный гидролиз протекает 6 ч, однако современные установки позволяют проводить процесс при повышенном давлении и, соответственно, более высокой температуре. При давлении 415–620 кПа и температуре до 160 °С крахмал гидролизуется в течение нескольких минут. Останавливают реакцию добавлением нейтрализующего реагента (обычно карбоната натрия), и pH повышается до 4-5,5
После гидролиза нерастворимые примеси, которые изначально присутствовали в крахмале, отделяют центрифугированием или фильтрованием, а растворимые примеси удаляют активированным углём и ионообменными смолами. Смолы также позволяют обесцветить полученную глюкозу. Конечный раствор упаривают. Большинство глюкозных сиропов продают в виде 70-85 % растворов, хотя их можно упарить и до твёрдого состояния[10].
Глюкозные сиропы отличаются по степени гидролиза крахмала: её оценивают по количеству присутствующих в конечном продукте восстанавливающих сахаров и выражают в декстрозных эквивалентах (DE). Интересно, что кислотный гидролиз является в целом случайным процессом, однако в данном случае при одинаковой степени конверсии получается очень воспроизводимый углеводный состав конечного продукта. В некоторых случаях этот факт является нежелательным ограничением, потому что производителю может понадобиться более гибко регулировать углеводный состав. Из-за этого в промышленности стали использовать ферментативный гидролиз крахмала[10].
Ферментативный гидролиз крахмала[править | править код]
Ферментативный гидролиз используют как дополнение к кислотному. Изначально таким способом пытались повысить степень конверсии и получить более сладкий и менее вязкий сироп с большим содержанием глюкозы. Однако ферментативный гидролиз позволяет также регулировать соотношение глюкозы и мальтозы в продукте. Для проведения ферментативного гидролиза pH повышают до 4-6, а температуру снижают до 60-70 °С, затем вносят необходимые ферменты, которые подбирают исходя из потребностей по составу. Бактериальные α-амилазы случайным образом расщепляют α-1,4-гликозидные связи в крахмале. β-Амилазы и грибковые α-амилазы расщепляют те же связи, но дают преимущественно мальтозу. Глюкоамилаза отщепляет по одной молекуле глюкозы с невосстанавливающего конца, но может расщеплять также α-1,6-связи. Пуллуланаза расщепляет α-1,6-связи. По окончании процесса ферменты дезактивируют нагреванием или изменением pH[10].
Открытие термоустойчивых α-амилаз позволило разработать полностью ферментативные процессы и ещё более точно контролировать степень конверсии и углеводный состав продукта. Ферменты вносят в суспензию крахмала при pH 6-6,5, после чего суспензию нагревают паром до 103-107 °С и выдерживают в течение 5-10 мин, а затем 1-2 ч при 95 °С. После этого проводят вторичный ферментативный гидролиз, как и в случае кислотного гидролиза[10].
Производство общего сахара[править | править код]
Большая часть глюкозы продаётся в виде сиропов, но существует небольшая потребность также в твёрдой глюкозе. Её производят как в чистом виде, так и в виде общего сахара (англ. total sugars) — отверждённого гидролизата крахмала. Общий сахар может содержать значительное количество мальтозы (DE<20), быть практически чистой глюкозой (95-99 %), а также содержать определённый процент фруктозы[11].
Производство кристаллической глюкозы[править | править код]
Изначально чистую кристаллическую глюкозу производили из крахмала, гидролизованного в кислой среде. В таких условиях удавалось добиться только 88 % содержания глюкозы, поскольку в условиях гидролиза образовывались побочные продукты, связанные с мутаротацией и изомеризацией. С 1938 года начали использовать ферментативный гидролиз, который позволил получать более чистую глюкозу[12].
Моногидрат α-D-глюкозы получают кристаллизацией из перенасыщенных сиропов с содержанием твёрдого вещества в 74-79 %, из которого глюкоза составляет 95-96 %. Такие сиропы производят ферментативным гидролизом, нацеленным на максимальную конверсию. Сироп охлаждают до 46-50 °С и смешивают с затравочными кристаллами из предыдущей партии. Сироп медленно охлаждают до 20-40 °С в течение 2-5 дней: при этом около 60 % кристаллизуется в виде моногидрата α-D-глюкозы. Маточный раствор отделяют на центрифугах, кристаллы глюкозы промывают водой и там же сушат до максимально сухого состояния (14 % влаги). Затем их досушивают потоком горячего воздуха до 8,5-9 % влаги (теоретическое содержание воды в моногидрате — 9,08 %). Кристаллизации не мешает наличие примесей, поэтому маточный раствор концентрируют и получают вторую порцию кристаллов либо объединяют его со следующей партией сиропа. Извлечение моногидрата глюкозы из сиропа достигает 87,5 %. При повторных кристаллизациях из маточного раствора степень выделения повышается до 100 %[12].
Безводную α-D-глюкозу кристаллизуют при 60-65 °С в условиях вакуума и испарения растворителя. Исходные сиропы должны быть достаточно чистые. Цикл кристаллизации значительно короче, чем для моногидрата, и составляет 6-8 ч. Выделяют и сушат кристаллы примерно так же, как описано выше. Содержание воды в конечном продукте не превышает 0,1 %[12].
Безводную β-D-глюкозу получают кристаллизацией выше 100 °С. Дополнительные сложности связаны с тем, что β-D-глюкоза значительно лучше растворима в воде, чем α-D-глюкоза (72 % против 30 % при 25 °С)[12].
Глюкоза может восстанавливаться в шестиатомный спирт (сорбит). Окисление глюкозы в зависимости от метода окисления может приводить к трём продуктам: глюконовой кислоте (окисление альдегидной группы), глюкаровой кислоте (дополнительно окисляется первичная OH-группа) либо глюкуроновой кислоте (окисление только первичной OH-группы)[8].
Как восстанавливающий сахар, глюкоза проявляет восстановительные свойства. Это проявляется в реакциях с реактивом Толленса (аммиачным раствором оксида серебра), реактивом Бенедикта и реактивом Фелинга (реагенты на основе меди).
Глюкоза — основной продукт фотосинтеза, образуется в цикле Кальвина.
В организме человека и животных глюкоза является основным и наиболее универсальным источником энергии для обеспечения метаболических процессов. Глюкоза является субстратом гликолиза, в ходе которого она может окислиться либо до пирувата в аэробных условиях, либо до лактата в случае анаэробных условий. Пируват, полученный таким образом в гликолизе, далее декарбоксилируется, превращаясь в ацетил-КоА (ацетилкоэнзим А). Также в ходе окислительного декарбоксилирования пирувата восстанавливается кофермент НАД+. Ацетил-КоА далее используется в цикле Кребса, а восстановленный кофермент используется в дыхательной цепи.
Глюкоза депонируется у животных в виде гликогена, у растений — в виде крахмала, полимер глюкозы — целлюлоза является основной составляющей клеточных оболочек всех высших растений. У животных глюкоза помогает пережить заморозки. Так, у некоторых видов лягушек перед зимой повышается уровень глюкозы в крови, за счёт чего их тела способны выдержать заморозку во льду.
Глюкозу используют при интоксикации (например, при пищевом отравлении и инфекциях), вводят внутривенно струйно и капельно, так как она является универсальным антитоксическим средством. Также препараты на основе глюкозы и сама глюкоза используются эндокринологами при определении наличия и типа сахарного диабета у человека (в виде стресс-теста на ввод повышенного количества глюкозы в организм).
- ↑ Рабинович В. А., Хавин З. Я. Краткий химический справочник. — 2-е издание. — Химия, 1978.
- ↑ Степаненко Б. Н., Городецкий В. К., Ковалев Г. В. Глюкоза // Большая медицинская энциклопедия : в 30 т. / гл. ред. Б. В. Петровский. — 3 изд. — Москва : Советская энциклопедия, 1978. — Т. 6. Гипотериоз — Дегенерация. — 528 с. — 150 000 экз.
- ↑ 1 2 3 4 5 Ullmann, 2006, p. 45–48.
- ↑ Терней, 1981, с. 444–447.
- ↑ 1 2 Робертс Дж., Касерио М. Основы органической химии / Пер. с англ. Ю. Г. Бунделя, под ред. А. Н. Несмеянова. — М. : Мир, 1978. — С. 10–27.
- ↑ 1 2 3 Терней, 1981, с. 424–429.
- ↑ 1 2 3 Ullmann, 2006, p. 48.
- ↑ 1 2 3 4 5 Химическая энциклопедия, 1988.
- ↑ Ullmann, 2016, p. 49–51.
- ↑ 1 2 3 4 5 Ullmann, 2016, p. 51–56.
- ↑ Ullmann, 2016, p. 56.
- ↑ 1 2 3 4 Ullmann, 2016, p. 56–58.
| Общие: | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Геометрия | |||||||||||||||
| Моносахариды |
| ||||||||||||||
| Мультисахариды | |||||||||||||||
| Производные углеводов | |||||||||||||||
Сахароза — Википедия
Материал из Википедии — свободной энциклопедии
Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 апреля 2019; проверки требуют 3 правки. Текущая версия страницы пока не проверялась опытными участниками и может значительно отличаться от версии, проверенной 20 апреля 2019; проверки требуют 3 правки. Эта статья — о химическом веществе. О пищевом продукте см. Сахар.| Сахароза | |
|---|---|
 ( {{{картинка}}}) | |
 ( ({{{изображение}}}) | |
| Систематическое наименование | (2R,3R,4S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-дигидрокси-2,5-бис(гидроксиметил)оксолан-2-ил]окси-6-(гидроксиметил)оксан-3,4,5-триол |
| Сокращения | α-D-глюкопиранозил-(1,2)-β-D-фруктофуранозид |
| Традиционные названия | свекловичный сахар, тростниковый сахар |
| Хим. формула | C12H22O11 |
| Состояние | Твёрдое, кристаллическое |
| Молярная масса | 342,2965 ± 0,0144 г/моль |
| Плотность | 1,587 г/см³ |
| Температура | |
| • плавления | 186 °C |
| • разложения | 367 ± 1 °F[1] и 320 ± 1 °F[1] |
| Давление пара | 0 ± 1 мм рт.ст.[1] |
| Растворимость | |
| • в воде | 211,5 г/100 мл |
| Рег. номер CAS | 57-50-1 |
| PubChem | 5988 |
| Рег. номер EINECS | 200-334-9 |
| SMILES | |
| InChI | 1S/C12h32O11/c13-1-4-6(16)8(18)9(19)11(21-4)23-12(3-15)10(20)7(17)5(2-14)22-12/h5-11,13-20H,1-3h3/t4-,5-,6-,7-,8+,9-,10+,11-,12+/m1/s1 |
| RTECS | WN6500000 |
| ChEBI | 17992 |
| ChemSpider | 5768 |
| NFPA 704 |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
 Медиафайлы на Викискладе Медиафайлы на Викискладе | |
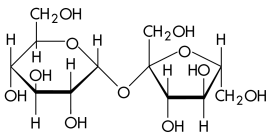
Сахаро́за (сукро́за, тростниковый сахар) C12H22O11, в быту просто сахар, — дисахарид из группы олигосахаридов, состоящий из двух моносахаридов: α-глюкозы и β-фруктозы.
Сахароза является весьма распространённым в природе дисахаридом. Она встречается во многих фруктах, плодах и ягодах. Особенно велико содержание сахарозы в сахарной свёкле и сахарном тростнике, которые и используются для промышленного производства пищевого сахара.
Сахароза, попадая в кишечник, быстро гидролизуется альфа-глюкозидазой тонкой кишки на глюкозу и фруктозу, которые затем всасываются в кровь. Ингибиторы альфа-глюкозидазы, такие, как акарбоза, тормозят расщепление и всасывание сахарозы, а также и других углеводов, гидролизуемых альфа-глюкозидазой, в частности, крахмала. Это используется в лечении сахарного диабета 2-го типа[2].
В чистом виде — бесцветные моноклинные кристаллы. При застывании расплавленной сахарозы образуется аморфная прозрачная масса — карамель. Сахароза имеет высокую растворимость. Растворимость (в граммах на 100 грамм растворителя): в воде 179 (0 °C) и 487 (100 °C), в этаноле 0,9 (20 °C). Малорастворима в метаноле. Не растворима в диэтиловом эфире. Плотность 1,5879 г/см3 (15 °C). Удельное вращение для D-линии натрия: 66,53 (вода; 35 г/100г; 20 °C). Температура плавления 186℃.
Не проявляет восстанавливающих свойств — не реагирует с реактивами Толленса, Фелинга и Бенедикта. Не образует открытую форму, поэтому не проявляет свойств альдегидов и кетонов. Наличие гидроксильных групп в молекуле сахарозы легко подтверждается реакцией с гидроксидами металлов. Если раствор сахарозы прилить к гидроксиду меди(II), образуется ярко-синий раствор сахарата меди. Альдегидной группы в сахарозе нет: при нагревании с аммиачным раствором оксида серебра(I) она не дает реакцию «серебряного зеркала», при нагревании с гидроксидом меди(II) не образует красного оксида меди(I). Из числа изомеров сахарозы, имеющих молекулярную формулу С12Н22О11, можно выделить мальтозу и лактозу.
Реакция сахарозы с водой[править | править код]
Если прокипятить раствор сахарозы с несколькими каплями соляной или серной кислоты и нейтрализовать кислоту щелочью, а после этого нагреть раствор, то появляются молекулы с альдегидными группами, которые и восстанавливают гидроксид меди(II) до оксида меди(I). Эта реакция показывает, что сахароза при каталитическом действии кислоты подвергается гидролизу, в результате чего образуются глюкоза и фруктоза:
- C12h32O11+h3O→C6h22O6+C6h22O6{\displaystyle {\mathsf {C_{12}H_{22}O_{11}+H_{2}O\rightarrow C_{6}H_{12}O_{6}+C_{6}H_{12}O_{6}}}}
Реакция сахарозы с гидроксидом меди(II)[править | править код]
В молекуле сахарозы имеется несколько гидроксильных групп. Поэтому соединение взаимодействует с гидроксидом меди (II) аналогично глицерину и глюкозе. При добавлении раствора сахарозы к осадку гидроксида меди (II) он растворяется; жидкость окрашивается в синий цвет. Но, в отличие от глюкозы, сахароза не восстанавливает гидроксид меди (II) до оксида меди (I).
Природные и антропогенные источники[править | править код]
Содержится в сахарном тростнике, сахарной свёкле (до 28 % сухого вещества), соках растений и плодах (например, берёзы, клёна, дыни и моркови). Источник получения сахарозы — из свёклы или из тростника, определяют по соотношению содержания стабильных изотопов углерода 12C и 13C. Сахарная свёкла имеет C3-механизм усвоения углекислого газа (через фосфоглицериновую кислоту) и предпочтительно поглощает изотоп 12C; сахарный тростник имеет C4-механизм поглощения углекислого газа (через щавелевоуксусную кислоту) и предпочтительно поглощает изотоп 13C.
Мировое производство в 1990 году — 110 000 000 тонн.
Статичное 3D-изображение
молекулы сахарозы-

Кристаллы коричневого
(нерафинированного тростникового) сахара
Сложные вещества — урок. Химия, 8–9 класс.
Химические элементы входят в состав сложных веществ (химических соединений).
Сложными называют вещества, состоящие из атомов разных химических элементов.
Большинство химических веществ являются сложными.
Многие сложные вещества имеют молекулярное строение. К молекулярным относятся метан Ch5, вода h3O, углекислый газ CO2, серная кислота h3SO4, глюкоза C6h22O6. Пластмассы, белки, жиры, крахмал тоже представляют собой сложные вещества, состоящие из молекул.
Модель молекулы воды

Модель молекулы глюкозы
Немолекулярное строение имеет песок SiO2, а также все сложные вещества, в состав которых входят металлы: поваренная соль NaCl, мел CaCO3, питьевая сода NaHCO3 и многие другие. Из сложных веществ немолекулярного строения состоят минералы и горные породы.

Модель кристалла поваренной соли
При определённых условиях сложные вещества можно разложить на несколько новых веществ. Так под действием электрического тока вода разлагается на водород и кислород, а сахар при нагревании превращается в уголь и воду.
Водород и кислород совсем не похожи на воду. При обычных условиях водород и кислород представляют собой газы, а вода — жидкость. Уголь и вода ничем не напоминают сахар.
Обрати внимание!
Свойства сложного вещества не являются суммой свойств веществ, образующихся при его разложении.
Сахара, класс простые — Справочник химика 21
К углеводам относятся многие соединения, обладающие более сложной структурой, чем простые сахара. Большинство углеводов, встречающихся в природе, состоит из двух или более молекул сахаров. Названия различных классов углеводов показывают, из какого числа молекул простого сахара (моносахаридов) состоит молекула углевода (например, дисахариды и трисахариды), в то время как термины олигосахариды и полисахариды используются для обозначения соединений, содержащих мало или много моносахаридных фрагментов. Хотя многие полисахариды построены из гексоз, также хорошо известны полисахариды, содержащие тетрозы и пентозы. [c.280]Углеводы удобно делить на два больших класса простые сахара и моносахариды (мономеры) и очень сложные полимеры этих простых сахаров, называемые полисахаридами. [c.256]
И все же качество — это не просто сумма свойств. Оно выражает целостную характеристику объекта, показывает функциональное единство его свойств, его внешней и внутренней определенности. Если мы просто перечислим свойства белый, сладкий, растворимый в воде, хрупкий, —то такое сочетание свойств еще не означает, что речь идет именно о сахаре. Подобным набором свойств могут обладать и другие химические вещества. Поэтому для идентификации вещества необходимо знать его индивидуальные свойства. Выделение из многообразия свойств наиболее существенных, общих для какого-то класса объектов, и в то же время отличающих его от других объектов, позволяет без труда установить принадлежность объекта к данному классу. [c.23]
Калорийность пищи, знакомая всем, следящим за своим весом, есть приведенная теплота сгорания, выраженная в ккал/г. Работники питания и диетологи вместо слова килокалория говорят просто калория , а иногда большая калория . Поэтому когда они говорят, что калорийность сахара составляет, допустим, 4 кал/г, то в действительности они имеют в виду 4 ккал/г. В среднем ценность физиологического горючего пищевых продуктов трех основных классов такова углеводы — 4 ккал/г, белки — 4 ккал/г и жиры — 9 ккал/г. [c.85]
Углеводы или сахариды — природные соединения, структура которых может быть, как правило, выражена общей формулой С,1(Н20) 1. Углеводы удобно разделять на два больших класса 1) мономеры, т. е. простые сахара или моносахариды 2) очень сложные полимеры этих простых сахаров, называемые полисахаридами, например крахмал, целлюлоза, декстрин, гликоген. [c.420]
Простейшие сахара (моносахариды) и их олигомеры и полимеры (полисахариды) составляют один из главных классов клеточных компонентов, объединяемых под общим названием углеводов. Типичным мономерным звеном служит а-О-глюкоза (а-глюкопираноза)—циклическая форма глюкозы [c.106]
УГЛЕВОДЫ (глюциды, глициды)—важнейший класс органических соединений, распространенных в природе, состав которых соответствует общей формуле С (НзО) — По химическому строению У.— альдегидо- или кетоноспирты. Различают простые У.— моносахариды (сахара), например глюкоза, фруктоза, и сложные—полисахариды, которые делят на низкомолекулярные У.— дисахариды (сахароза, лактоза и др.) и высокомолекулярные, такие, например, как крахмал, клетчатка, гликоген. Характерным для У. является то, что моносахариды не гидролизуют, а молекулы полисахаридов при гидролизе расщепляются на две молекулы (дисахариды) или на большее число молекул (крахмал, клетчатка) моносахаридов. У. имеют огромное значение в обмене веществ организмов, являясь главным источником [c.255]
Исключительно важная роль, которую играют гликозиды, и особенно 0-гликозиды, в химии и биохимии углеводов, выдвигает синтез гликозидов на первый план в синтетической химии производных сахаров по гликозидному центру. Материал, изложенный в зтой главе, позволяет сделать следующую общую оценку состояния зтой проблемы. Синтез простейших гликозидов всех типов в настоящее время разработан подробно и обычно не составляет сложной задачи. Для синтеза 1,2-транс-гли коз идо в всех типов разработано несколько достаточно общих методов, которые в большинстве случаев позволяют синтезировать 1,2-/иранс-гликозиды с довольно сложными агликонами, в том числе и большинство природных гликозидов. Однако обших методов синтеза 1,2-/ ис-гликозидов со сложными агликонами не существует, и разработка таких методов для гликозидов всех классов, особенно О-гликозидов, является центральной задачей синтетической химии в этой области. Как видно из изложенного материала, синтезу 1,2-/ ис-глюкозидов препятствует соучастие соседних групп, применяемых для защиты спиртовых гидроксилов сахара. Поэтому можно ожидать, что эта задача будет решена путем разработки эффективных методов защиты спиртовых гидроксилов сахара группировками, неспособными к соучастию и удаляемыми без разрушения или изменения гликозидной связи в синтезируемых производных. С другой стороны, вероятно, потребуется разработка эффективных путей активации заместителя при гликозидном центре, способного реагировать с агликонами достаточно быстро, в мягких условиях и со строгим стереохимическим контролем. [c.233]
Структурно-химический признак, позволяющий объединить такие, казалось бы несходные по своим свойствам, вещества, как сахар, крахмал, клетчатку в один класс соединений, будет выяснен в дальнейшем — после знакомства с некоторыми сравнительно простыми представителями углеводов. [c.170]
В процессе изложения материала преподаватель как бы следует по генетической цепи углеводов сначала моносахариды— простейшие сахара (глюкоза, фруктоза), затем второй класс углеводов — сахароподобные дисахариды (сахароза) и в заключение третий класс углеводов— полисахариды, не обладающие свойствами сахаров (крахмал, клетчатка). [c.138]
Согласно К. Фрейденбергу, природные таннины делятся на два больших класса гидролизующиеся таннины и конденсированные, или катехиновые, таннины. Таннины первой категории дают в результате гидролиза минера
Простые сахара (простые углеводы): что это, список, вред
Простые сахара естественным образом содержатся во фруктах и молоке, или их можно производить в промышленных масштабах и добавлять в пищу для подслащивания, предотвращения порчи или улучшения структуры и текстуры.
В этой статье объясняются различные виды простых сахаров, как их идентифицировать на этикетках продуктов питания и как они могут повлиять на ваше здоровье.

Простые сахара (углеводы) – что это такое, их воздействие на здоровье и потенциальный вред
Что такое простые сахара?
Углеводы – это молекулы, которые содержат одну, две или несколько молекул сахара, называемых сахаридами (1).
Они поставляют четыре калории на грамм и являются предпочтительным источником энергии для вашего организма.
Существует два основных типа углеводов: простые и сложные. Разница между ними заключается в количестве содержащихся в них молекул сахара.
Простые углеводы – также известные как простые сахара – содержат одну или две молекулы сахара, тогда как сложные углеводы имеют три или более молекулы.
Простой сахар может быть моно- или дисахаридом.
Моносахариды
Моносахариды – это самые простые углеводы, так как ваш организм дальше не может их расщеплять.
Это позволяет вашему организму усваивать их быстро и легко, за исключением фруктозы.
Существует три типа моносахаридов (1):
- Глюкоза: Фрукты и овощи являются естественными источниками глюкозы. Она также часто встречается в сиропах, конфетах, меде, спортивных напитках и десертах.
- Фруктоза: Основным естественным диетическим источником фруктозы являются фрукты и ягоды, поэтому фруктозу обычно называют фруктовым сахаром.
- Галактоза: Основным диетическим источником галактозы является лактоза – сахар, присутствующий в молоке и молочных продуктах, таких как сыр, сливочное масло и йогурт.
Дисахариды
Дисахариды состоят из двух молекул сахара или двух моносахаридов, связанных вместе.
Ваш организм должен расщепить связанные моносахариды, прежде чем они могут быть усвоены.
Существует три типа дисахаридов (1):
- Сахароза (глюкоза + фруктоза): Сахароза – чаще всего называемая столовым сахаром – это натуральный подсластитель, полученный из сахарной свёклы или сахарного тростника. Он добавляется в пищу во время обработки и естественным образом содержится во фруктах и овощах.
- Лактоза (глюкоза + галактоза): Также известная как молочный сахар, лактоза содержится в молоке и молочных продуктах.
- Мальтоза (глюкоза + глюкоза): Мальтоза содержится в солодовых напитках, таких как пиво и солодовые напитки.
Резюме:
Простые сахара содержат одну или две молекулы сахара. Углевод с одной молекулой сахара называется моносахаридом, тогда как углевод с двумя молекулами сахара, связанными вместе, является дисахаридом.
Слишком много добавленных сахаров может нанести вред вашему здоровью
Для многих людей слово «сахар» имеет негативный оттенок.
Многие продукты с высоким содержанием питательных веществ, такие как фрукты и овощи, естественным образом содержат сахар, и их не следует избегать, так как они приносят пользу вашему здоровью.
С другой стороны, добавленные сахара – например, в сладких напитках, конфетах, выпечке и десертах – могут способствовать возникновению многих проблем со здоровьем.
Добавленные сахара были связаны с повышением уровня развития ожирения, сердечно-сосудистых заболеваний и повышенным риском развития рака.
Связаны с ожирением
Ожирением страдают почти 40% взрослых людей, проживающих во многих развитых странах (2).
Это связано с серьезными рисками для здоровья, включая сахарный диабет, болезни сердца и рак.
Кроме того, ожирение очень дорого лечить. По сравнению с людьми со здоровым весом люди, страдающие ожирением, ежегодно тратят на здравоохранение тысячи долларов (3).
Это накладывает серьезное экономическое бремя на человека, на семьи и налогоплательщиков (4).
Причина ожирения широко обсуждается и носит многофакторный характер, но считается, что избыточное потребление добавленных сахаров играет основную роль (5, 6).
Добавленные сахара вносят дополнительные калории в ваш рацион, что со временем может привести к увеличению массы тела.
Сладкий вкус и вкусовая привлекательность могут усугубить чрезмерное потребление добавленного сахара по сравнению с другими питательными веществами, повышая риск увеличения массы тела (7, 8, 9, 10).
Может способствовать развитию болезни сердца
Сердечно-сосудистые заболевания являются основной причиной смерти во многих странах (11).
Это чаще всего вызвано атеросклерозом – заболеванием, при котором налет (холестериновые бляшки) на внутренних стенках кровеносных сосудов, которые ведут к вашему сердцу, заставляет их сужаться и затвердевать. Это уменьшает кровоток, что может привести к сердечному приступу (12, 13).
Несколько исследований показали, что получение слишком большого количества калорий из добавленного сахара может привести к повышению уровня триглицеридов – известного фактора риска развития сердечно-сосудистых заболеваний (14, 15, 16, 17).
Одно исследование показало, что люди, которые получали 10-25% калорий из добавленного сахара, имели на 30% больший риск смерти от болезней сердца по сравнению с теми, кто получал менее 10% калорий из добавленного сахара (18).
Более того, этот риск почти удваивается для тех, кто получает более 25% калорий из добавленного сахара.
Может увеличить риск развития рака
Избыток калорий из добавленных сахаров может увеличить воспаление и окислительный стресс.
Незначительное воспаление и окислительный стресс необходимы для хорошего здоровья, но слишком большое их количество может привести к ряду заболеваний и состояний, включая рак (19, 20, 21).
Во многих исследованиях сообщалось о повышенных маркерах воспаления – например, С-реактивного белка и мочевой кислоты – при потреблении добавленных сахаров (22, 23, 24).
Считается, что добавление сахара повышает риск развития рака, повышая уровень определенных гормонов, но эти эффекты еще недостаточно изучены (25, 26, 27).
Резюме:
Добавленные сахара были связаны с ожирением. Более того, они могут способствовать развитию сердечно-сосудистых заболеваний и повысить риск заболевания раком.
Как идентифицировать добавленные сахара на этикетках продуктов питания
Вы можете найти добавленные сахара в различных типах продуктов – даже в тех, которые вы не считаете сладкими, такие как кетчуп, хлеб и консервированную фасоль.
Тем не менее основными источниками добавленных сахаров являются подслащенные напитки, конфеты, десерты, мороженое и сладкие хлопья (28).
Изучите состав продукта на этикетке, чтобы узнать, сколько граммов сахара в нем содержится.
Исторически сложилось так, что на этикетках продуктов питания не различается содержащийся в них натуральный или добавленный сахар. Это затрудняет определение количества добавленного сахара.
American Heart Association рекомендует женщинам и мужчинам получать меньше 25 граммов и 38 граммов добавленного сахара в день из своего рациона соответственно (29).
Получение большего количества этих количеств затрудняет удовлетворение ваших потребностей в питательных веществах, оставаясь в пределах ваших суточных калорийных ограничений (30).
Изучение списка ингредиентов на продуктах также может помочь вам определить добавленные сахара.
Вот названия добавленных сахаров, которые вы можете найти на этикетках:
- Безводная (ангидридная) декстроза
- Коричневый сахар
- Сахарная пудра
- Кукурузный сироп
- Кукурузный сироп с высоким содержанием фруктозы
- Мед
- Кленовый сироп
- Меласса (чёрная патока)
- Нектар агавы
- Нерафинированный сахар
На этикетках перечислены ингредиенты в порядке убывания их веса, причем сначала используются ингредиенты, содержащиеся в наибольшем количестве, а затем в меньших количествах.
Это означает, что, если продукт содержит сахар в качестве первого ингредиента, вы знаете, что он содержит больше сахара, чем чего-либо еще.
Резюме:
Вы можете идентифицировать добавленные сахара, посмотрев на этикетку продукта и прочитав список ингредиентов. Ограничение получения ваших калорий от добавленных сахаров может помочь вам удовлетворить ваши потребности в питательных веществах, оставаясь при этом в пределах ваших суточных калорий.
Почему вы не должны полностью бояться простых сахаров
Нет сомнений в том, что сахар может быть вредным для вашего здоровья при употреблении в избытке.
Тем не менее сахар является лишь одним из компонентов вашего рациона питания. Наивно делать его полностью ответственным за ожирение и другие болезни и состояния в современном обществе (31).
Исследования показывают, что сахар вызывает проблемы со здоровьем только тогда, когда он присутствует в избыточном количестве в вашем рационе или если вы получаете больше калорий, чем вам нужно из сахара (10, 32, 33, 34).
Ограничение потребления подслащенных сахаром напитков, сладостей и десертов очень важно для хорошего здоровья, но полный отказ от куска пирога или порции вашего любимого мороженого – неправильный подход. Это не жизнеспособно, не приятно и не полезно для вашего здоровья.
Кроме того, простые сахара встречаются в природе в широком спектре здоровых продуктов, таких как фрукты, овощи и молочные продукты. Эти продукты приносят в ваш рацион целый ряд других важных питательных веществ, таких как витамины, минералы, антиоксиданты и клетчатка.
Резюме:
Сахар вреден для вашего здоровья, когда он составляет слишком большую часть вашего рациона или вы получаете лишние калории из сахара. Следовательно, ограничение, но не полное избегание сахара – особенно добавленного сахара – имеет смысл для вашего здоровья.
Подведем итог
- Простые сахара – это углеводы с одной (моносахарид) или двумя (дисахарид) молекулами сахара.
- Многие здоровые продукты, такие как фрукты и овощи, естественным образом содержат сахар, и их не следует избегать, так как они приносят пользу вашему здоровью. Тем не менее избыточное употребление сахара связано с ожирением и повышенным риском сердечно-сосудистых заболеваний и рака.
- Вы можете узнать, сколько сахара добавлено в продукт, посмотрев на его состав на этикетке.
- Несмотря на то, что добавленные сахара могут оказывать вредное воздействие на ваше здоровье, вы можете употреблять их в умеренных количествах и в качестве части здорового рациона питания.
Поделиться новостью в соцсетях Метки: Сахар, углеводы
 « Предыдущая запись
« Предыдущая запись  Следующая запись »
Следующая запись »